In Europa, il tumore dello stomaco è stato il più frequente fino alla metà del secolo scorso; negli ultimi decenni, ha registrato costanti diminuzioni nei tassi d’incidenza e mortalità. Le ragioni della diminuzione della mortalità per tumore dello stomaco in Europa sono complesse e non del tutto comprese. Tra queste, vi è il miglioramento dell’alimentazione, sia per quanto riguarda la varietà della dieta, sia per quanto riguarda la conservazione degli alimenti, in particolare, in seguito al diffondersi della refrigerazione; inoltre hanno influito la diminuita prevalenza dell’infezione da Helicobacter pylori nelle generazioni più recenti e la riduzione del fumo di sigarette.
Il processo neoplastico ha origine quasi sempre dalla mucosa, lo strato più interno della parete gastrica e viene classificato come adenocarcinoma, per distinguerlo da altre forme, più rare, che originano dagli strati più profondi della parete (i sarcomi e i tumori stromali o GIST), dal sistema linfatico (linfoma non Hodgkin primitivo), o di natura neuroendocrina (carcinoidi).
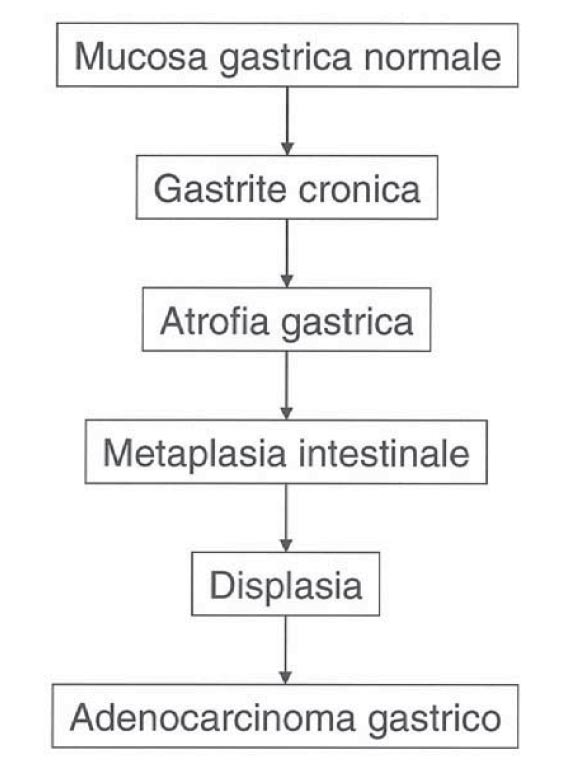
La maggior parte degli adenocarcinomi dello stomaco è di tipo intestinale e si sviluppa attraverso una cascata di condizioni e lesioni precancerose che sono la gastrite atrofica, la metaplasia intestinale e la displasia (Cascata di Correa, fig. 1). Una gestione appropriata dei pazienti con condizioni e lesioni precancerose è fondamentale per ridurre l’incidenza e la mortalità per cancro gastrico.